5a Lezione
4a Lezione
Idrossi acidi. Acido succinico, malico e tartarico. Acidi lattici.




3a Lezione
Lezione ed Esercitazione
Gruppi funzionali. Installazione e utilizzo di software in chimica organica. Funzioni principali. Molecole in 3d. Alcoli a 4 atomi di carbonio di formula molecolare C4H10O. Isomeria strutturale. Relazione tra struttura e proprietà. Proprietà odorose degli alcoli di formula C4H10O. Soluzioni etanoliche al 10% di 1-butanolo, 2-butanolo, 2-metil-1-propanolo, 2-metil-2-propanolo.
Aldeidi e chetoni. Nomenclatura.
Derivati degli acidi carbossilici: gli esteri. Componente acida e componente alcolica. Nomenclatura. Acetato di butile. Butirrato di butile.

Derivati degli acidi carbossilici: le ammidi. Differenza tra ammine ed ammidi. La risonanza. Molecole organiche contenenti il gruppo amminico come sostituente. Gli amminoacidi. I peptidi. Il legame ammidico. Assenza di rotazione attorno al legame ammidico.
Alogenuri alchilici.

Introduzione alla stereoisomeria. Alcheni. 1-butene, 2-butene. Isomeria geometrica. I simboli E e Z. Regole di Priorità. Applicazioni.
Polieni. Beta-carotene

2a Lezione
1a Lezione
1a Prova di esonero
1. Scrivere le strutture di Lewis delle molecole di seguito indicate e definire l’ibridazione dell’atomo di carbonio presente. a) anidride carbonica; b) carbonato di potassio; c) Bromotriclorometano; d) Acido cianidrico; e) Formaldeide; f) Acido formico. (4)
2. Dare i nomi alle molecole di seguito illustrate: (6)

3. Il nome IUPAC dell’amminoacido treonina presente nelle proteine è acido 2-ammino-3-idrossibutanoico. Scrivere tutti i possibili stereoisomeri ed indicare quelli appartenenti alla serie sterica L. (5)
4. Gli acidi bicarbossilici succinico, malico e tartarico sono tutti presenti in quantità variabili nei vini. Essi presentano rispettivamente 0, 1 e 2 ossidrili nella struttura che contiene complessivamente 4 atomi di carbonio. Scrivere la struttura e dare il nome IUPAC a tutti gli acidi. Indicare inoltre la presenza di eventuali centri chirali e scrivere i corrispondenti stereoisomeri. (8)
5. Indicare la relazione di isomeria esistente tra l’acido (2S,3R)-3-fluoro-2-idrossi butanoico 1 e le strutture a-f. (7)

Esame scritto
1. Scrivere le strutture delle seguenti molecole:
a) 2-cloro-3,4-diidrossipentanale; b) acido 3-amino-2-fluoro-4-nitrobenzoico; c) 2,2,3,3-tetrametilciclobutanone; d) (2E)-4,5-dimetil-2-esene; e) acido (2S,3R)-2-ammino-3-metilpentanoico ; f) Quanti stereoisomeri esistono della molecola e)?
2. Identificare i gruppi funzionali presenti nella vitamina C, la cui struttura è di seguito riportata
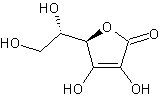
3. Scrivere ed elencare secondo acidità crescente le molecole di seguito elencate: a) 2-nitrofenolo; b) fenolo; c) 2-metil-ciclopropanolo; d) acido 3-fluorobutanoico; e) acido 2-cloropropanoico; f) metil-ciclobutano;
4. Dare una spiegazione del fatto che il cicloesene reagisce rapidamente con il bromo, mentre il benzene è inerte.
5. Scrivere la struttura di a) un D-amminoacido; b) un L-chetoesoso; c) un Trigliceride; d) un nucleoside; e) un estere.
CdL Viticoltura ed Enologia 19 Gennaio 2006
1. Dare il nome alle strutture mostrate.
2. Classificare i monosaccaridi le cui strutture sono di seguito indicate.
4. Come si potrebbero separare 1, 3,5-tribromo cicloesano dalla cicloesilammina?
5. Scrivere le strutture delle seguenti sostanze: a) un D-amminoacido; b) Un L-aldopentoso; c) Il trigliceride formato dall’acido butirrico. (6)
CdL in Scienze e Tecnologie Agrarie
Esame Scritto di Chimica Organica (21 Luglio ’05)
1. Scrivere le strutture delle seguenti molecole:
a) 2,3-diidrossi-4-metilesanale; b) (2S) acido 2-ammino-3-metilpentanoico; c) 1,2-dimetilciclobutanolo; d) (2E,4Z)-2,4-esadiene; e) Acido 2,4-dimetil-3-nitrobenzoico.
2. Disegnare tutti i possibili stereoisomeri dell’acido 2,3-diidrossi-butandioco.
3. Scrivere ed elencare secondo acidità crescente le molecole di seguito elencate: a) 2-nitrofenolo; b) 4-metilfenolo; c) 2-metil-cicloesanolo; d) acido 2-fluoropropanoico; e) acido 3-iodoesanoico; f) 1,1,2-trimetilciclopropano.
4. Spiegare perché l’idrocarburo 1,3-ciclopentadiene si comporta come un acido (pKa ≈ 15) mentre il ciclopentene no (pKa ≈40).
5. Scrivere la struttura di a) un L-amminoacido; b) un D-chetopentoso; c) un monogliceride; d) un nucleotide; e) un acetale.
2a prova di esonero CHIMICA ORGANICA
CdL Viticoltura ed Enologia 18 Dicembre 2006
6. Dare il nome alle strutture mostrate, spiegando la scala di acidità osservata.
7. Classificare i monosaccaridi le cui strutture sono di seguito indicate.
8. Indicare quali tra le specie chimiche proposte di seguito può definirsi aromatica.
9. Illustrare un metodo per separare la 3,5-dietilanilina dal 1,3-dietilbenzene.
10. Scrivere le strutture delle seguenti sostanze: a) un dipeptide formato solo da D-amminoacidi; b) Gli anomeri di un D-aldotreoso chiuso in forma furanosica;c) Il digliceride formato dall’acido butirrico.
CdL Viticoltura ed Enologia
ESAME SCRITTO DI CHIMICA ORGANICA 19 febbraio 2007
11. Dare un nome alle molecole di seguito indicate, specificando per ognuna il numero degli stereoisomeri possibili.
12. Indicare quali caratteristiche deve possedere una molecola organica per definirsi aromatica.
13. Illustrare un metodo per separare l’acido 3-metilbenzoico dal clorobenzene.
14. Scrivere le strutture generiche delle seguenti sostanze: a) un D-aldochetoso; b) un b-ammino acido; c) il trigliceride formato dall’acido butirrico; d) un emiacetale ciclico; e) un nucleoside presente nel DNA; f) un acido grasso monoinsaturo.
15. Scrivere ed elencare secondo basicità crescente le strutture delle molecole di seguito mostrate. a) Etilammina; b) Diisopropilammina; c) Ammoniaca; d) Anilina; e) 4-nitroanilina; f) 1,3,5-trimetilbenzene.
Esame scritto
1. Scrivere le strutture delle seguenti molecole:
a) 3,4-dicloroeptanale; b) acido 3-amino-2-cloro-4-etilbenzoico; c) 1,2,2-trimetilcicloutanolo; d) (2Z)-4-metil-2 pentene; e) 5-metilciclopent-2-en-1-amino; f) Quanti stereoisomeri esistono della molecola e)?
2. Identificare tutti i gruppi funzionali presenti nella vitamina A, (retinolo), la cui struttura è di seguito riportata.

4. Spiegare la differenza di acidità osservata nel propano CH3-CH2-CH3 (pKa =50) il propilene, CH3-CH=CH2 (pKa= 40) e il propino CH3-C≡CH (pKa=30).
5. Scrivere la struttura di a) un L-amminoacido; b) un D-chetoesoso; c) un digliceride; d) un nucleoside; e) un estere.
Esame scritto
1. Scrivere le strutture delle seguenti molecole:
a) 2,3-diidrossi-4-metilesanale; b) (2S) acido 2-ammino-3-metilpentanoico; c) 1,2-dimetilciclobutanolo; d) (2E,4Z)-2,4-esadiene; e) Acido 2,4-dimetil-3-nitrobenzoico.
2. Disegnare tutti i possibili stereoisomeri dell’acido 2,3-diidrossi butandioco.
3. Scrivere ed elencare secondo acidità crescente le molecole di seguito elencate: a) 2-nitrofenolo; b) 4-metilfenolo; c) 2-metil-cicloesanolo; d) acido 2-fluoropropanoico; e) acido 3-iodoesanoico; f) 1,1,2-trimetilciclopropano.
4. Spiegare perché l’idrocarburo 1,3-ciclopentadiene si comporta come un acido (pKa ≈ 15) mentre il ciclopentene no (pKa ≈40).
5. Scrivere la struttura di a) un L-amminoacido; b) un D-chetopentoso; c) un monogliceride; d) un nucleotide; e) un acetale.
Programma di Chimica Organica
CFU 4
gli studenti devono usare l'indirizzo: luilongo@gmail.com
Testo consigliato:
Obiettivi formativi:
Il corso si prefigge di fornire le basi conoscitive della teoria strutturale delle molecole organiche al fine di comprendere ed interpretare la diversità molecolare dei prodotti naturali e quella derivante dalla loro trasformazione chimica ed enzimatica.
Prerequisiti:
Chimica Generale ed Inorganica
Programma:
Introduzione alla chimica organica. Gli atomi, il carbonio, le molecole. Orbitali, legami, ibridazione. Formule di Lewis. La risonanza. Idrocarburi saturi ed insaturi. Classi di composti organici. Nomenclatura. Utilizzo di Software in chimica organica. Isomeria strutturale. Geometria cis-trans. Stereochimica assoluta e relativa. Chiralità. Enantiomeri e diastereoisomeri. Aromaticità e composti aromatici. Acidità e basicità in chimica organica. Amminoacidi peptidi e proteine. Carboidrati. Acetali. Monosaccaridi e polisaccaridi. Acidi Nucleici. Lipidi.












